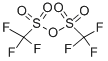
| Описание |
Трифлуорометансулфоновият анхидрид, известен също като трифличен анхидрид, се е доказал като изключителен реагент за широк спектър от трансформации. Като търговски и лесно достъпен реагент, той е широко използван в синтетичната химия поради високата си електрофилност. Като се има предвид неговия висок афинитет към О-нуклеофили, реакцията с алкохоли, карбонили, серен фосфор и йодни оксиди към образуването на съответните трифлати е силно благоприятна. Като една от водещите напускащи групи в органичната химия, генерираните трифлати след това отварят вратата за различни трансформации надолу по веригата, включително (но не само) реакции на заместване, процеси на кръстосано свързване, редокс реакции и пренареждания [1-2] . |
| Химични свойства |
бистра безцветна до светлокафява течност |
| Употреби |
Трифлуорометансулфоновият анхидрид е силен електрофил, използван в химичния синтез за въвеждане на трифлиловата група. |
| Употреби |
Трифлуорометансулфоновият анхидрид се използва за превръщане на феноли и имин в трифличен естер и NTf група. Това е силен електрофил, използван за въвеждане на трифлилова група в химическия синтез. Той служи като реагент при получаването на алкил и винил трифлати и за стереоселективен синтез на донори на манозазид метил уронат. Той действа като катализатор за гликозилиране с аномерни хидрокси захари за получаване на полизахариди. |
| Определение |
ChEBI: Triflic анхидридът е органосулфонов анхидрид. Той е функционално свързан с трифлинова киселина. |
| Профил на реактивност |
Електрофилното активиране на третични и вторични амиди с трифликов анхидрид (Tf2O; рифлуорометансулфонов анхидрид) при меки условия води до съответно иминиеви и имино трифлати, които могат да се използват като универсални реагенти за реакция с различни C-, N-, O- и S -нуклеофили за превръщането на амидна функция в различни продукти. Други съдържащи кислород нуклеофили, като сулфоксиди и фосфорни оксиди, също биха могли да претърпят нуклеофилна атака с Tf2O за генериране на тиониев трифлат, електрофилни P-видове и фосфониев трифлат. Тези силно активни преходни видове могат лесно да претърпят реакции на нуклеофилно заместване за по-нататъшни различни трансформации. Освен това, поради силното електрофилно свойство, Tf2O е склонен да реагира с относително слаби нуклеофили като нитрилни групи или някои азотсъдържащи хетероциклични съединения. В допълнение, Tf2O също се използва като ефективен реагент за радикално трифлуорометилиране и трифлуорометилтиолиране чрез освобождаване на SO2 или процес на деоксигениране за синтеза на трифлуорометилирани и трифлуорометилтиолирани съединения[2]. |
| Опасност |
Може да е корозивен за металите. Опасен за поглъщане. Причинява тежки изгаряния на кожата и увреждане на очите. |
| Запалимост и експлозивност |
Не е класифициран |
| Синтез |
Синтезът на трифлуорометансулфонов анхидрид е както следва:
Суха, {{0}} ml., облодънна колба се зарежда с 36,3 g. (0.242 mol) трифлуорометансулфонова киселина (Забележка 1) и 27,3 g. (0,192 мола) фосфорен пентоксид (Бележка 2). Колбата се затваря и се оставя да престои на стайна температура поне 3 часа. През този период реакционната смес се променя от каша в твърда маса. Колбата е снабдена с дестилираща глава с къс път и се нагрява първо с поток от горещ въздух от топлинен пистолет и след това с пламък от малка горелка.Колбата се нагрява, докато престане да дестилира трифлуорометансулфонов анхидрид, т.к. 82-115 градуса, като се получават 28,4-31,2 g. (83–91%) от анхидрида, безцветна течност. Въпреки че този продукт е достатъчно чист за използване в следващия етап, останалата киселина може да бъде отстранена от анхидрида чрез следната процедура. Каша от 3,2 g. фосфорен пентаоксид в 31,2 g. от суровия анхидрид се разбърква при стайна температура в запушена колба в продължение на 18 часа. След като реакционната колба е снабдена с дестилираща глава с къс път, тя се нагрява с маслена баня, като се получава 0.7 g. на предшественика, bp 74–81 градуса, последван от 27,9 g. от чистия анхидрид на трифлуорометансулфонова киселина, т.к. 81–84 градуса.

|
| съхранение |
Съхранявайте на хладно, сухо и добре проветриво място. Чувствителен към влага. |
| Методи за пречистване |
Може да се приготви прясно от безводна киселина (11,5 g) и P2O5 (11,5 g, или половината от това тегло) чрез оставяне на стайна температура за 1 час, дестилиране на летливи продукти, след което се дестилира през къса колона на Vigreux. Той лесно се хидролизира от H2O и се разлага значително след няколко дни, за да освободи SO2 и да произведе вискозна течност. Съхранявайте го на сухо при ниски температури. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Препратки |
[1] Хаоци Джан. „Трифлуорометансулфонов анхидрид в амидно активиране: мощен инструмент за изковаване на хетероциклични ядра.“ TCIMAIL (2021).
[2] Д-р Qixue Qin, проф. д-р Ning Jiao, Zengrui Cheng. „Последни приложения на трифлуорометансулфонов анхидрид в органичния синтез.“ Angewandte Chemie 135 10 (2022). |