
представяне на продукта
| Калциев флуорид Основна информация |
| Химични свойства кристална структура Употреби Производствен метод |
| Име на продукта: | Калциев флуорид |
| Синоними: | Калциев флуорид; калциев флуорид, 99,9% следи от метали; калциев флуорид, 99,95% следи от метали; калциев флуорид, безводен, ампулиран под аргон, 99,99% следи от метали; калциев флуорид в Китай; ANTI-CNOT8 (C-TERM) антитяло произведени в заек;CAF1-подобен протеин;CALIFp |
| CAS: | 7789-75-5 |
| MF: | CaF2 |
| MW: | 78.07 |
| EINECS: | 232-188-7 |
| Категории продукти: | Неорганични вещества; метален халид |
| Mol файл: | 7789-75-5.mol |
 |
|
| Калциев флуорид Химични свойства |
| Точка на топене | 1402 градуса |
| Точка на кипене | 2500 градуса (осветени) |
| плътност | 3,18 g/mL при 25 градуса (осветено) |
| индекс на пречупване | 1.434 |
| Рп | 2500 градуса |
| температура на съхранение | -20 степен |
| разтворимост | Слабо разтворим в киселина; неразтворим в ацетон. |
| форма | прът |
| цвят | бяло |
| Специфично тегло | 3.18 |
| Разтворимост във вода | 0.015 g. на 100g H20 при стайна температура. (НЕРАЗТВОРИМ) |
| Чувствителен | Хигроскопичен |
| Мерк | 14,1667 |
| Продуктова константа на разтворимост (Ksp) | pKsp: 8.28 |
| Граници на експозиция | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2,5 mg/m3 |
| Диелектрична константа | 2,5 (околна) |
| Стабилност: | Стабилен. Калциевият флуорид е инертен към органични химикали и много киселини, включително HF. Бавно ще се разтвори в азотна киселина. |
| InChIKey | WUKWITHWXAAZEY-UHFFFAOYSA-L |
| Референция на база данни на CAS | 7789-75-5(справка на база данни на CAS) |
| Справочник по химия на NIST | Калциев флуорид (7789-75-5) |
| EPA Система за регистър на веществата | Калциев дифлуорид (7789-75-5) |
| Информация за безопасност |
| Кодове за опасност | Xi, Xn |
| Изявления за риска | 36/37/38 |
| Изявления за безопасност | 26-37/39-36 |
| РИДАДР | 3288 |
| WGK Германия | 1 |
| RTECS | EW1760000 |
| Бележка за опасност | Дразнещ |
| TSCA | да |
| Код по ХС | 28261900 |
| Данни за опасни вещества | 7789-75-5(Данни за опасни вещества) |
| токсичност | LD50 ip при мишки: 2638,27 mg/kg (Stratmann) |
| Информация за MSDS |
| Доставчик | език |
|---|---|
| Калциев флуорид | английски |
| Сигма Олдрич | английски |
| АКРОС | английски |
| АЛФА | английски |
| Използване и синтез на калциев флуорид |
| Химични свойства | Калциевият флуорид е основната съставка на флуорита или флуорита, химическата формула е CaF2, представлява безцветен кубичен кристал или бял прах. Относителната плътност е 3,18, точката на топене е 1423 градуса, точката на кипене е около 2500 градуса. Разтворимостта във вода е минимална, 100 g вода може да разтвори само 0,0016 g при 18 градуса, неразтворима е в ацетон, но разтворима в солна киселина, флуороводородна киселина, сярна киселина, азотна киселина и разтвор на амониева сол и не може да реагира с разреден киселина, но може да реагира с гореща концентрирана сярна киселина и да генерира флуороводородна киселина, може да образува комплекс, когато се разтвори в разтвор на алуминиеви и железни соли (Fe3 +). Естественият калциев флуорид е минерален флуорит или флуорит, често показва сиви, жълти, зелени, лилави и други цветове, понякога е безцветен, прозрачен, лъскаво стъкло, крехък и относителната плътност е 3,01 ~ 3,25, има значителен феномен на флуоресценция. Може да се използва като източник на флуор и материал за получаване на система от флуороводородна киселина, флуорид; и може да се използва и по отношение на производството на стъкло, емайл, глазура. Флуоритът се използва главно като флюс в металургията, много чистият флуорит може да се използва за направата на специални лещи. Водата, когато съдържа (1~1,5) × 10-6 калциев флуорид, може да предотврати проблеми със зъбите. Освен това може да се използва при топене на желязо и стомана, производство на химикали, стъкло, керамика. Чистият продукт може да се използва за катализатор на дехидратация, дехидрогениране. Чрез въздействието на разтворими калциеви соли (калциев карбонат или калциев хидроксид) и натриев флуорид или флуороводородна киселина могат да се получат амониев флуорид, калциев флуорид. |
| кристална структура | Калциевият флуорид е йонен кристал с флуорни аниони в прост кубичен масив и калциеви катиони в половината от кубичните места на структурата. Калциевите йони също могат да се разглеждат като намиращи се върху „разширена“ fcc решетка с флуорните йони, причиняващи разделянето на решетката им да бъде 0.39 nm. Това представяне е показано на долната диаграма. Единичната клетка има 4 Ca2+йони и 8 F1-йони.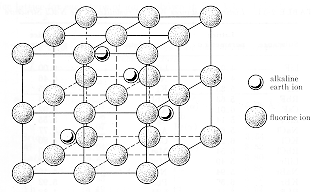 Материалът е прозрачен във видимата спектрална област и показва електронна оптична адсорбция в ултравиолетовата и решетъчна оптична абсорбция в инфрачервената. |
| Употреби |
Индустрия
Приложение
Роля/полза
Химическо производство
Производство на флуороводородна киселина и флуорид
Суровина/източник на флуорид
Производство на флуорни фини химикали и синтетичен криолит
Суровина/източник на флуорид
Архитектурен материал
Производство на стъкло
Флусиращ агент/насърчаване на топенето на суровини
Производство на цимент
Минерализиращо средство
Производство на керамична глазура
Флюсове и оцветители
Металургия
Топене на желязо и стомана, производство на феросплави и др.
Флусиращ агент/намалява точката на топене на огнеупорни вещества
Лекарство
Лечение, контрол, профилактика и подобряване на алергичните реакции
Насърчаване на образуването на нова кост
Термични системи за изобразяване, спектроскопия, телескопи и ексимерни лазери
Производство на оптични компоненти, като прозорци и лещи
Суровина/широк диапазон от честоти на предавателна светлина; нисък индекс на пречупване; висока термостабилност
други
Производство на заваръчни средства
Важни компоненти в покритията на заваръчни пръти и прахове за заваряване
Дехидратация и реакция на дехидрогениране
Катализатор/ускоряване на процеса на реакция
Производство на спирачни накладки
Добавка/помага за намаляване на абразията, причинена от висока топлина и триене
|
| Метод на производство | Депозитите на флуорит, открити в Китай, се използват основно в мината, като се използва метод за подземен добив или плитък открит добив и подземен дълбок добив, за най-наклонената вена на рудното тяло, разширението също е голямо. Методът за добив се основава на метода на свиване на плитки дупки. Минният процес вижда "фосфатна скала". Методите за обогатяване обикновено имат два типа, единият е сурова руда, която може да се превърне в квалифициран руден концентрат чрез обработка на избрани, вторият е ръчно избрана постна руда и хвост. |
| Описание | Калциевият флуорид е безцветно кристално или бяло прахообразно вещество. Молекулно тегло{{0}}.08;Специфично тегло (H2O:1)=3.18 при 20 градуса; Точка на кипене=2495 степен; Точка на замръзване/топене=1423 градуса. Идентификация на опасността (въз основа на NFPA-704 M Рейтингова система): Здраве 2, Запалимост 0, Реактивност 0. Практически неразтворим във вода. |
| Химични свойства | Калциевият флуорид, CaF2, известен също като флуорит и фелдшпат, е безцветно твърдо вещество, съставено от кубични кристали. Има ниска разтворимост във вода, но е лесно разтворим в разтвори на амониева сол. Калциевият флуорид се използва при синтеза на флуороводородна киселина и при ецване на стъкло. Калциевият флуорид не е хигроскопичен и е относително инертен. Той има достатъчно висока устойчивост на термичен и механичен удар и лесно се произвежда в различни геометрии на детектори. Калциевият флуорид има много ниско налягане на парите, което му позволява да се използва в голямо разнообразие от вакуумни приложения. Той е неразтворим във вода и повечето органични разтворители, което позволява радиоактивни проби в разтвор да бъдат поставени в пряк контакт с кристала. Калциевият флуорид е прозрачен материал, използван за откриване на -лъчи до няколкостотин keV и за откриване на заредени частици. Поради ниския си атомен номер, фотофракцията на материала е относително малка, което ограничава използването му в спектрометрия с лъчи при по-високи енергии. Ниският атомен номер обаче прави калциевия флуорид идеален материал за откриване на -частици поради малкото обратно разсейване. |
| Физични свойства | Бял кубичен кристал или прах; индекс на пречупване 1.434; плътност 3,18 g/cm3; твърдост 4 по Моос; топи се при 1418 градуса; изпарява се при 2,533 градуса; неразтворим във вода (16 mg/L при 20 градуса); Ksp 3,9x10-11; слабо разтворим в разредена минерална киселина; разтворим в концентрирани киселини (с реакция). |
| Употреби | Естествено срещащият се CaF2 е основният източник на флуороводород, стоков химикал, използван за производството на широка гама от материали. Флуоридът се освобождава от минерала чрез действието на концентрирана сярна киселина: CaF2 (твърд)+H2SO4 (течен)→CaSO4 (твърд)+2HF (газ) CaF2 се използва като оптичен компонент поради неговата химическа стабилност при неблагоприятни условия. Калциевият флуорид обикновено се използва като материал за прозорец както за инфрачервени, така и за ултравиолетови дължини на вълната, тъй като е прозрачен в тези региони (около 0).15 до 9 mm) и показва изключително нисък индекс на пречупване. Калциевият флуорид е водонеразтворим източник на калций за използване в чувствителни към кислород приложения, като например производство на метали. В изключително ниски концентрации (ppm) флуоридните съединения се използват в здравни приложения. Флуоридните съединения също имат значителни приложения в синтетичната органична химия. Те също така често се използват за легиране на метали и за оптично отлагане. Използва се и като флюс за топене и течна обработка на желязо, стомана и техните композити. Действието му се основава на сходната му точка на топене с желязото, способността му да разтваря оксиди и способността му да омокря оксиди и метали. |
| Употреби | Флуорът е основният първичен източник на флуор и неговите съединения. В черната металургия се използва като флюс за повишаване на течливостта на шлаката. Стоманодобивната промишленост е най-големият потребител; химическата промишленост, второ и стъклото и керамиката, трето. Синтетичният флуорид се използва в оптичната индустрия (пропуска ултравиолетови лъчи), а чистият калциев флуорид се използва като катализатор при дехидратиране и дехидрогениране. Използва се за флуориране на питейна вода. |
| Употреби | Калциевият флуорид е търговски важен източник на флуоридни съединения, както и флуороводород. Той е прозрачен от ултравиолетовата до инфрачервената област. Използва се в спектроскопия, системи за термично изображение и ексимерни лазери; използва се и в производството на оптични компоненти, включително прозорци, призми и лещи. В допълнение, той се използва и в алуминиевата металургия, производството на спирачни накладки и в зъбния емайл. |
| Определение | Чиста естествено срещаща се форма на калциев флуорид. |
| Производствени методи | Търговският продукт се получава от естествено срещащ се минерален флуорипат, който е пречистен и стрит на прах. Също така може да се утаи чрез смесване на разтвор на натриев флуорид с разтворима калциева сол: Ca (NO3)2+ 2NaF → CaF2+ NaNO3 Алтернативно, може да се получи чрез третиране на калциев карбонат с флуороводородна киселина: СаСО3+ 2HF → CaF2+ CO2 + H2O. |
| Определение | Минерална форма на калциев флуорид (CaF2), използвани при производството на някои цименти и видове стъкло. |
| Общо описание | Сив прах или гранули без мирис. Потъва във вода. |
| Профил на реактивност | Калциевият флуорид има слаба окислителна или редуцираща сила. Редокс реакциите обаче все още могат да възникнат. По-голямата част от съединенията в този клас са слабо разтворими или неразтворими във вода. Ако са разтворими във вода, тогава разтворите обикновено не са нито силно киселинни, нито силно основни. Тези съединения не реагират с вода. |
| Опасност | Дразнител. |
| Опасност за здравето | Слаба остра токсичност |
| Запалимост и експлозивност | Незапалим |
| Промишлени употреби | Наричан още флуорит, флуоритът е кристален или масивен гранулиран минерал със състав CaF2, използван като флюс при производството на стомана, за производство на флуороводородна киселина, в опалесциращо стъкло, в керамични емайли, за извиване на изкуствен криолит, като свързващо вещество за стъкловидни абразивни колела и в производството на бял цимент. Това е по-добър флюс за стомана от варовика, като прави течна шлака и освобождава желязото от сяра и фосфор. Киселинният шпат е вид, използван при производството на флуороводородна киселина. Използва се също за производство на хладилни агенти, пластмаси и химикали, както и за намаляване на алуминия. Оптичният флуорипат е най-високият клас, но не е често срещан. Флуоридните кристали за оптични лещи се отглеждат изкуствено от киселинен флуорипат. Чист калциев флуорид, Ca2F6, е безцветен кристален прах, използван за ецване на стъкло, в емайли и за намаляване на триенето в машинни лагери. Използва се и за керамични части, устойчиви на флуороводородна киселина и повечето други киселини. Калциевият флуорит има силиций в молекулата и е кристален прах, използван за емайли. Прозрачните ромбични флуоридни кристали, използвани за трансформиране на електрическа енергия в светлина, са оловен флуорид, PbF2. |
| Профил на безопасност | Умерено токсичен при интраперитонеално приложение. Леко токсичен при поглъщане. Експериментален тератоген. Други експериментални репродуктивни ефекти. Докладвани са данни за мутация. Вижте също ФЛУОРИДИ и КАЛЦИЕВИ СЪЕДИНЕНИЯ. При нагряване до разлагане отделя токсични изпарения на F-. |
| Потенциално излагане | Калциевият флуорид се използва за производството на флуороводородна киселина; като поток при производството на стомана; при топене; електродъгово заваряване, изработка на стъкло и керамика; и за флуориране на питейната вода. |
| Първа помощ | Ако този химикал попадне в очите, незабавно свалете всички контактни лещи и незабавно ги напойте в продължение на най-малко 15 минути, като от време на време повдигате горните и долните клепачи. Незабавно потърсете медицинска помощ. Ако този химикал влезе в контакт с кожата, свалете замърсеното облекло и го измийте незабавно със сапун и вода. Незабавно потърсете медицинска помощ. Ако този химикал е бил вдишан, отстранете експозицията, започнете спасително дишане (използвайки универсални предпазни мерки, включително маска за реанимация), ако дишането е спряло и CPR, ако сърдечната дейност е спряла. Трансфер незабавно до медицинско заведение. Когато този химикал бъде погълнат, потърсете медицинска помощ. Лекар или упълномощен парамедик може да обмисли прилагането на гел от алуминиев хидроксид, ако е в съзнание. |
| съхранение | Цветов код-зелен: Може да се използва общо съхранение. Съхранявайте в плътно затворени контейнери на хладно, добре проветриво място, далеч от киселини и химически активни метали (като калий, натрий, магнезий и цинк), тъй като ще се получи корозивен флуороводород. |
| Доставка | Калциевият флуорид не е специално обхванат от DOT в неговите стандарти за опаковане, ориентирани към ефективността. |
| Несъвместимости | Прахът може да образува експлозивна смес с въздуха. Реагира с вода, влажен въздух и пара, освобождавайки запалим водороден газ; и може да се самозапали във въздуха. Силен редуциращ агент; несъвместим с окислители (хлорати, нитрати, пероксиди, перманганати, перхлорати, хлор, бром, флуор и др.); контактът може да причини пожар или експлозия. Да се пази от алкални материали, силни основи, силни киселини, оксокиселини, епоксиди. Несъвместим с метални халогени, сребърен флуорид и тетрахидрофуран |
| Продукти и суровини за получаване на калциев флуорид |
| Суровини | Hydrogen fluoride-->Calcium hydroxide-->CARBON MONOXIDE-->Quartz-->Calcium acetate-->калциев магнезиев фосфат (CMP) |
| Продукти за приготвяне | Hydrogen fluoride-->Boron trifluoride diethyl etherate-->Potassium Phosphate Monobasic-->Hexafluorosilicic acid-->Calcium cyanamide-->Sodium fluoride-->Trisodium hexafluoroaluminate-->Aluminum fluoride-->bastnasite-->Carbon tetrafluoride-->cryolite-->ZINC SILICOFLUORIDE-->МАГНЕЗИЕВ ХЕКСАФЛУОРАЦЕТИЛАЦЕТОНАТ ДИХИДРАТ |
Популярни тагове: цинков флуорид, Китай цинков флуорид производители, доставчици, фабрика
Един чифт: Циркониев флуорид
Следваща: Калциев флуорид
Може да харесаш също
Изпрати запитване


