| Описание |
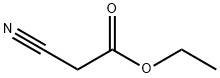
Етилцианоацетатът е етилов естер на цианооцетната киселина. Етил цианоацетатът се хидролизира бързо при неутрални и алкални условия до цианооцетна киселина и етанол (и така се случва при повечето физиологични условия и условия на околната среда), докато при кисело рН полуживотът е значително по-дълъг.
Съобщава се за кондензация на Кневенагел на етил цианоацетат с алдехид. Докладва се засилена с микровълни кондензационна реакция на Knoevenegal на етил цианоацетат с алдехид, P2O5, пиперидин и хлоробензен. |
| Химични свойства |
Етилцианоацетатът е безцветна до сламенокафява течност с лека приятна миризма |
| Употреби |
Етилцианоацетатът може да се използва при синтеза на етилглиоксилат. Той беше използван за изследване на реакциите на кондензация на Knoevenagel в микрореактор с използване на зеолитни катализатори, получени чрез присаждане на аминогрупи върху NaX и CsNaX зеолити. |
| Употреби |
Реагент, използван при белязан пиримидин и синтез на пурин. Етилцианоацетатът е естер. Може да се използва в синтеза на етил глиоксилат. Използва се за изследване на реакциите на кондензация на Knoevenagel в микрореактор с използване на зеолитни катализатори, получени чрез присаждане на аминогрупи върху NaX и CsNaX зеолити. |
| Подготовка |
Етилцианоацетатът може да се получи чрез действието на натриев или калиев цианид върху етилхлороацетат и чрез действието на натриев цианид върху натриев хлороацетат, последвано от естерификация. |
| Общо описание |
Безцветна течност. По-плътен от вода. Контактът може да раздразни кожата, очите и лигавиците. Точка на възпламеняване 210 градуса F. Може да бъде токсичен при поглъщане. Използва се за производство на други химикали. |
| Въздушни и водни реакции |
Слабо разтворим във вода. |
| Профил на реактивност |
Етилцианоацетатът е едновременно нитрил и естер. Естерите реагират с киселини, за да освободят топлина заедно с алкохоли и киселини. Силните окислителни киселини могат да причинят бурна реакция, която е достатъчно екзотермична, за да запали реакционните продукти. Топлина се генерира и от взаимодействието на естери с каустични разтвори. Запалимият водород се генерира чрез смесване на естери с алкални метали и хидриди. Нитрилите могат да полимеризират в присъствието на метали и някои метални съединения. Несъвместими са с киселини; смесването на нитрили със силни окислителни киселини може да доведе до изключително бурни реакции. Нитрилите обикновено са несъвместими с други окислители като пероксиди и епоксиди. Комбинацията от основи и нитрили може да произведе циановодород. Нитрилите се хидролизират във воден разтвор на киселина и основа, за да се получат карбоксилни киселини (или соли на карбоксилни киселини). Тези реакции генерират топлина. Пероксидите превръщат нитрилите в амиди. Нитрилите могат да реагират енергично с редуциращи агенти. Ацетонитрилът и пропионитрилът са разтворими във вода, но нитрилите, по-високи от пропионитрила, имат ниска разтворимост във вода. Те също са неразтворими във водни киселини. |
| Опасност |
Токсичен при поглъщане и вдишване. |
| Опасно за здравето |
ТОКСИЧЕН; вдишване, поглъщане или контакт (кожа, очи) с изпарения, прах или вещество може да причини тежки наранявания, изгаряния или смърт. Контактът с разтопено вещество може да причини сериозни изгаряния на кожата и очите. Реакцията с вода или влажен въздух ще отдели токсични, корозивни или запалими газове. Реакцията с вода може да генерира много топлина, която ще увеличи концентрацията на изпарения във въздуха. Пожарът ще произведе дразнещи, корозивни и/или токсични газове. Изтичането от вода за контрол на пожара или вода за разреждане може да бъде корозивно и/или токсично и да причини замърсяване. |
| Опасност от пожар |
Запалим материал: може да гори, но не се запалва лесно. Веществото ще реагира с вода (някои бурно), освобождавайки запалими, токсични или корозивни газове и изтичане. При нагряване изпаренията могат да образуват експлозивни смеси с въздуха: опасност от експлозия на закрито, на открито и в канализацията. Повечето изпарения са по-тежки от въздуха. Те ще се разпространяват по земята и ще се събират в ниски или затворени зони (канализация, мазета, резервоари). Парите могат да се придвижат до източника на запалване и да избухнат обратно. При контакт с метали може да се отдели запалим водороден газ. Контейнерите могат да експлодират при нагряване или ако са замърсени с вода. |
| Профил на безопасност |
отров чрез поглъщане. Умерено токсичен при интраперитонеално и подкожно приложение. Запалим, когато е изложен на топлина или пламък; може да реагира с окисляващи материали. Wdl реагира с вода или пара, за да произведе токсични и запалими пари. За гасене на пожар използвайте CO2, сух химикал. При нагряване до разлагане или при контакт с киселина или киселинни изпарения той отделя силно токсични изпарения от CN-. Вижте също НИТРИЛИ. |
| Потенциално излагане |
Нитрил, използван за производство на бои, фармацевтични продукти и други химикали. |
| Първа помощ |
Ако този химикал попадне в очите, незабавно свалете всички контактни лещи и ги напоявайте незабавно поне 15 минути, като от време на време повдигате горните и долните клепачи. Незабавно потърсете медицинска помощ. Ако този химикал влезе в контакт с кожата, свалете замърсеното облекло и незабавно измийте със сапун и вода. Незабавно потърсете медицинска помощ. Ако този химикал е бил вдишан, отстранете експозицията, започнете спасително дишане (използвайки универсални предпазни мерки, включително маска за реанимация), ако дишането е спряло и CPR, ако сърдечната дейност е спряла. Прехвърлете незабавно до медицинско заведение. Когато този химикал бъде погълнат, потърсете медицинска помощ. Дайте големи количества вода и предизвикайте повръщане. Не карайте човек в безсъзнание да повръща |
| съхранение |
повторно местоположение на отровата. Преди да работите с този химикал, трябва да сте обучени за правилното му боравене и съхранение. Съхранявайте в плътно затворени контейнери на хладно, добре проветриво място, далеч от окислители, силни основи, силни киселини, редуциращи агенти, влага и източници на запалване. Когато е възможно, автоматично изпомпвайте течност от варели или други контейнери за съхранение към контейнерите за обработка |
| Доставка |
UN3276 Нитрили, течни, токсични, н.у., клас на опасност: 6.1; Етикети: 6.1-Отровни материали, изисква се техническо наименование, потенциална опасност при вдишване (Специална разпоредба 5). |
| Методи за пречистване |
Естерът се разклаща няколко пъти с воден 10% Na2CO3, промива се добре с вода, изсушава се с Na2SO4 и се дестилира фракционно. [Beilstein 2 IV 1889.] |
| Несъвместимости |
Несъвместим с окислители (хлорати, нитрати, пероксиди, перманганати, перхлорати, хлор, бром, флуор и др.); контактът може да причини пожар или експлозия. Да се пази от алкални материали, силни основи, силни киселини, оксокиселини, епоксиди и редуциращи агенти. Нитрилите могат да полимеризират в присъствието на метали и някои метални съединения. Несъвместими са с киселини; смесването на нитрили със силни окислителни киселини може да доведе до изключително бурни реакции. Нитрилите обикновено са несъвместими с други окислители като пероксиди и епоксиди. Комбинацията от основи и нитрили може да произведе циановодород. Нитрилите се хидролизират във воден разтвор на киселина и основа, за да се получат карбоксилни киселини (или соли на карбоксилни киселини). Тези реакции генерират топлина. Пероксидите превръщат нитрилите в амиди. Нитрилите могат да реагират енергично с редуциращи агенти. Ацетонитрилът и пропионитрилът са разтворими във вода, но нитрилите, по-високи от пропионитрила, имат ниска разтворимост във вода. Те също са неразтворими във водни киселини. Реагира с влага, вода и пара, образувайки токсични изпарения. |
| Изхвърляне на отпадъци |
Консултирайте се с регулаторните агенции по околната среда за насоки относно приемливи практики за изхвърляне. Генераторите на отпадъци, съдържащи този замърсител (по-големи или равни на 100 kg/mo) трябва да отговарят на разпоредбите на EPA, регулиращи съхранението, транспортирането, обработката и изхвърлянето на отпадъци. |