
представяне на продукта
| Хипофосфорна киселина Основна информация |
| Схема Химични свойства Употреби Токсичност ИДЕНТИФИКАЦИЯ НА ОПАСНОСТИТЕ Метод на приготвяне Метод на производство |
| Име на продукта: | Хипофосфорна киселина |
| Синоними: | ХИПОФОСФОРНА КИСЕЛИНА, 30% (W/V) РАЗТВОР; ХИПОФОСФОРНА КИСЕЛИНА, 50% (W/V) РАЗТВОР; Хипофосфорна киселина: (Фосфинова киселина); Хипофосфорна киселина, 50% w/w aq. разтвор;хипофосфорна;хипофосфорна киселина(корозивнатечност,киселина,неорганична,нос);хипофосфорна киселина,50%w/вод.разтвор.;РАЗТВОР НА ХИПОФОСФОРНА КИСЕЛИНА 50% ВОДЕН |
| CAS: | 6303-21-5 |
| MF: | HO2P |
| MW: | 63.980501 |
| EINECS: | 228-601-5 |
| Категории продукти: | HPA;Неорганични;6303-21-5 |
| Мол файл: | 6303-21-5.mol |
 |
|
| Хипофосфорна киселина Химични свойства |
| Точка на топене | -25 степен |
| Точка на кипене | 108 градуса (759,8513 mmHg) |
| плътност | 1,206 g/mL при 20 градуса (осветено) |
| налягане на парите | <17 mmHg ( 20 °C) |
| температура на съхранение | без ограничения. |
| разтворимост | много разтворим в H2O, етанол, етилов етер |
| pka | pK1 1.1. |
| форма | хигроскопични кристали или безцветна маслена течност |
| цвят | Безцветен |
| Разтворимост във вода | РАЗТВОРИМО |
| Мерк | 13,4894 |
| Стабилност: | Стабилен. Несъвместим със силни основи. Реагира бурно с окислители, силни основи, живачен (II) нитрат и живачен (II) оксид. Не нагрявайте над 100 С. |
| InChIKey | GQZXNSPRSGFJLY-UHFFFAOYSA-N |
| Референция на база данни на CAS | 6303-21-5(справка на база данни на CAS) |
| Справочник по химия на NIST | Хипофосфорна киселина (6303-21-5) |
| EPA Система за регистриране на вещества | Фосфинова киселина (6303-21-5) |
| Информация за безопасност |
| Кодове за опасност | C |
| Изявления за риска | 34 |
| Изявления за безопасност | 26-36/37/39-45 |
| РИДАДР | UN 3264 8/PG 3 |
| WGK Германия | 1 |
| RTECS | SZ6400000 |
| TSCA | да |
| Клас на опасност | 8 |
| PackingGroup | II |
| Код по ХС | 28111990 |
| Данни за опасни вещества | 6303-21-5(Данни за опасни вещества) |
| Информация за MSDS |
| Доставчик | език |
|---|---|
| Фосфинова киселина | английски |
| Сигма Олдрич | английски |
| АКРОС | английски |
| АЛФА | английски |
| Използване и синтез на хипофосфорна киселина |
| Контур | Хипофосфористата киселина е известна още като "хипофосфит". Това е безцветно масло или кристал, важен фин химически продукт. Основната употреба е като редуциращ агент за безелектрическо покритие, фосфорът предотвратява обезцветяването на смоли, може също да се използва в катализатора на реакцията на естерификация, хладилния агент, по-специално за производството на продукт с висока чистота натриев хипофосфит. Има няколко метода за получаване, общият промишлен метод за производство е методът на йонообменна смола и методът на електродиализа. Химичните свойства на хипофосфорната киселина, употребите, токсичността и производствените методи са редактирани от andy от Chemicalbook. (2016-12-04) |
| Химични свойства | Представлява разтопяващи се кристали или безцветно масло. Точка на топене: 26,5 градуса. Относителна плътност (специфично тегло): 1,439 (твърдо, 19 градуса). Разтворим е във вода, етанол и етер и може да се смесва във всякакви пропорции с вода, етанол, ацетон. Във въздуха лесно се разтваря до сиропообразна течност, а водният разтвор е кисел. Хипофосфорната киселина е едноосновна киселина, във воден разтвор, Хипофосфорната киселина е силна киселина, Ka=10-2 (25 градуса); той е относително стабилен при стайна температура; реакцията на диспропорциониране може да продължи при 130 градуса, да се разложи на фосфин и фосфорна киселина: 2H3PO2=H3PO4+PH3 Има силна редукция, разтворът на соли на тежки метали може да бъде възстановен до метали като Cu2 +, Hg2 +, Ag +, като например: 4Ag+H3PO2+2H2)=4Ag+H3PO4+4H+ Той е слаб окислител, може да се редуцира до фосфин, фосфин, когато срещне силен редуциращ агент. |
| Употреби | 1. Хипофосфористата киселина се използва като редуциращ агент за безелектрическо покритие; 2. Може да се използва за предотвратяване на обезцветяване на смола от фосфорна киселина; 3. Използва се като катализатор на естерификация, хладилен агент; 4. Използва се за производство на хипофосфит, натриеви соли, манганови соли, железни соли обикновено се използват като подхранващи вещества; 5. Хипофосфорната киселина се използва в медицината и като редуциращ агент, определянето на арсен, телур и отделянето на тантал, ниобий и други реагенти. 6. Той е силен редуциращ агент, може да се използва за получаване на натриев хипофосфит, калциев фосфат и други хипофосфити. 7. Може да се използва за баня за покритие. Фармацевтични продукти. редуциращ агент. общи реактиви. 8. Той е силен редуциращ агент, може да се използва при производството на натриев хипофосфит, калциев фосфат и други хипофосфити. 9. Този продукт се използва широко като редуциращ агент, Ag, Cu, Ni, Hg и други метали се редуцират до съответния метал, за проверка на As, Nb, Ta и други реагенти, той може да се използва за получаване на Na , K, Ca, Mn, Fe и други видове хипофосфит. |
| токсичност | Той е негорим. Но когато контактува с дупка H агент, това ще предизвика пожар. При среща с окислител може да възникне бурна реакция и горене. Когато се нагрее до висока степен, той може да се разложи на силно токсичен фосфинов газ или дори да експлодира. Той е разяждащ. Хипофосфористата киселина често се добавя в безалкохолни напитки и тъй като не се абсорбира. Така че рискът е малък, но особено силният хипофосфит наранява стомашно-чревния тракт. Случайно попадне в очите или в контакт с кожата, измийте обилно с вода. Производствените оператори трябва да носят защитно облекло и друго защитно облекло. Производственото оборудване трябва да бъде запечатано, работилницата трябва да се вентилира добре. |
| ИДЕНТИФИКАЦИЯ НА ОПАСНОСТИТЕ | Предупреждение за опасност: Причинява тежки изгаряния на кожата и увреждане на очите. Причинява сериозно увреждане на очите Препоръки за безопасност: Не вдишвайте прах/дим/газ/мъгла/пари/спрей. Измийте обилно след работа. Носете защитни ръкавици и защита за очи/лице. ПРИ ПОГЛЪЩАНЕ: Изплакнете устата. НЕ предизвиквайте повръщане. ПРИ КОНТАКТ С КОЖАТА (или косата): Отстранете/свалете незабавно всички замърсени дрехи. Изплакнете кожата с вода/душ. ПРИ ПОПАДАНЕ В ОЧИТЕ: Изплакнете внимателно с вода в продължение на няколко минути. Свалете контактните лещи, ако налични и лесни за изпълнение. Продължете изплакването. ПРИ ВДИШВАНЕ: Изведете пострадалия на чист въздух и го поставете в покой в удобна за дишане позиция. Незабавно се обадете в ЦЕНТЪР ПО ТОКСИКОЛОГИЯ или лекар/лекар. Съхранявайте заключено. Изхвърлете този материал и неговия контейнер в пункт за събиране на опасни или специални отпадъци. |
| Начин на приготвяне | 1. Разтворът на фосфор и бариев хидроксид се нагрява, може да се генерира бариева сол Ba (H2PO2) 2 • 2H2O, сярна киселина се добавя към разтвор на барий на хипофосфорна киселина, Ba2+ може да се утаи: Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2 Хипофосфорната киселина може да се получи чрез изпаряване при понижено налягане и кристализация при ниска температура. Поради това, че в този процес разтворимостта на бариевата сол е малка, така че концентрацията на получената хипофосфорна киселина не е висока, промишленият продукт трябва да се пречиства чрез прекристализация. 2. бариевият оксид (или вар) и разтворът на бял фосфор се нагряват заедно, за да се образува вторичен бариев фосфат (или калций), след което реагира със сярна киселина, филтрува се, концентрира се, за да се получи продукт, или се получава разтвор на натриев хипофосфит H- тип йонообменна смола може да извлече продукт. Този метод изисква голямо количество смола, а етапът на регенериране и измиване на смола е тромав, обикновено струва повече от $7 на паунд, подходящ е само за производство на малки партиди и не е подходящ за широкомащабни промишлени приложения. 3. Хипофосфорната киселина се приготвя чрез метод на електродиализа, при който електродиализната клетка се разделя на три части, те са анодна камера, камера за суровини и катодна камера, междинният продукт е разделен от анионна мембрана и катионна мембрана, между две мембрани се поставя разтвор на натриев хипофосфит (концентрация от 100g/L~500g/L), анодната камера е разреден разтвор на хипофосфорна киселина 5g/L, анодната камера е разреден разтвор на натриев хидроксид (5g/L), между полюсите преминава DC (3V~36V), анод освобождава кислород и генерира вторичен продукт от хипофосфорна киселина; катодът отделя водород и генерира вторичен продукт от натриев хидроксид, времето за реакция е 3 ~ 21 часа. Реакциите на анодната камера и катодната камера са както следва: анодна камера: H2O==H++OH- 2OH-==O2+2H2O+4e H++H2PO2-==H3PO2 катодна камера: H2O==H++OH- 2H++2e==H2 Na++OH-==NaOH Електродиализният метод на приготвяне Хипофосфорната киселина е прост и инвестицията в оборудване е малка, подходяща е за масово производство. 4. Започвайки от промишлен клас натриев хипофосфит, Cl-, SO42-аниони, които влияят на показателите за качество на хипофосфорната киселина, се отстраняват чрез утаяване, йоните на тежките метали се отстраняват от разтвора чрез образуване на сулфид и след това с помощта на силна киселина катионобменна смола за получаване на натриев вторичен фосфат, може да се получи продукт с висока чистота. Процесът може да произвежда висококачествен вторичен фосфат, технически е осъществим, процесът е прост, лесна работа, добро качество на продукта, може да отговори на нуждите на електронната промишленост, отбранителната промишленост и други високотехнологични области. 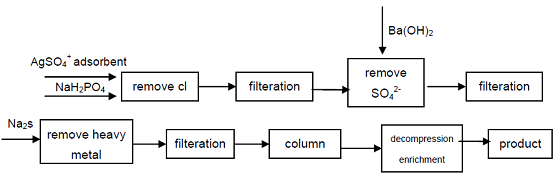 фигура 1 Процес на производство на хипофосфорна киселина от промишлен натриев хипофосфит. 5. Метод с йонообменна смола: около 70 g катионобменна смола, намокрена с вода, се опакова в стъклена тръба с 5 mol/L солна киселина, циркулираща около 15 минути, след щателно измиване с вода, воден разтвор на натриев хипофосфит с висока чистота (15 g/ 60 ml H2O) протича през нея, колоната със смола първо се промива с 50 ml, след това с 25 ml дестилирана вода. Изтичащата киселина и промивката се комбинират, концентрират се чрез изпаряване във водна баня. Концентрираната киселина се поставя във висок вакуум със сушилня P205 за дехидратиране, охлаждане и кристализация, филтриране, прекристализация, за получаване на продукт хипофосфорна киселина. |
| Метод на производство | Метод с йонообменна смола: поставете около 70 g водоразтворими катионобменни смоли, които да напълните в стъклена епруветка. Циркулирайте с 5 mol/L солна киселина за около 15 минути и промийте достатъчно с вода. Накарайте висоководен разтвор на натриев хипофосфит (15 g/60 ml H2O) да тече през колоната със смола, последвано от промиване първо с 50 ml вода и след това изплакване с 25 ml дестилирана вода. Изтичащата киселина и промивните води се комбинират и концентрират чрез изпаряване на водна баня. Концентрираната киселина се изпраща в сушилня с висок вакуум P205 за дехидратация, последвана от охлаждаща кристализация, филтриране и прекристализация за получаване на крайния продукт от хипофосфорна киселина. |
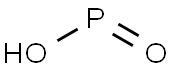
| Описание | Хипофосфорната киселина е мощен редуциращ агент с молекулна формула H3PO2. Неорганичните химици наричат свободната киселина с това име, въпреки че нейното наименование по IUPAC е дихидридохидроксидооксидофосфор или приемливото име на фосфинова киселина. Това е безцветно нискотопимо съединение, което е разтворимо във вода, диоксан и алкохоли. Формулата за хипофосфорната киселина обикновено се изписва H3PO2, но по-описателното представяне е HOP(O)H2, което подчертава нейния монопроточен характер. Солите, получени от тази киселина, се наричат фосфинати (хипофосфити). |
| Описание | Тази киселина има обща формула H4P2O6 и се различава от другите оксифосфорни киселини. Има много особености. Образува се заедно с фосфора и фосфорните киселини, когато фосфорът се окислява от влажен въздух. Ако белият фосфор се изложи на въздух и към образуваната течност се добави натриев ацетат, донякъде неразтворимият натриев хипофосфат Na2H2P2O6·6H2O се отделя. Натриевият хипофосфат монохидрат обаче е много разтворим и се разтваря при -98.7 g/100 ml. |
| Химични свойства | безцветна течност |
| Физични свойства | Безцветни течни кристали или маслена течност; кисела миризма; плътност 1,493 g/cm3; топи се при 26,5 градуса; кипи при 130 градуса ; много разтворим във вода, алкохол и етер; плътността на 50% воден разтвор е 1,13 g/mL. |
| Употреби | Хипофосфористата киселина се използва предимно за безелектродно никелиране. Той участва в редукцията на арендиазониевите соли. Той действа като добавка в реакциите на естерификация на Фишер. Също така, той служи като неутрализиращ агент, антиоксидант, катализатор при полимеризация и поликондензация и омокрящ агент. Освен това се използва при формулирането на фармацевтични продукти, обезцветяване на полимери, пречистване на вода и извличане на благородни или цветни метали. В допълнение към това, той се използва като избелващ агент за пластмаси, синтетични влакна, обезцветяващ агент и за стабилизиране на цвета по време на производството на химикали и няколко пластмаси. |
| Подготовка | Хипофосфорната киселина може да се получи по различни методи: 1. Кипяне на бял фосфор с калциев хидроксид: P4+ 4Ca(OH)2 + 8H2O → 4Ca(H2PO2)2 + 4H2 Калциевата сол е разтворима във вода. При обработка със сярна киселина се получава хипофосфорна киселина: (H2PO2)2Ca + H2ТАКА4 → 2H3PO2+ CaSO4 Продуктовата смес се филтрира за отстраняване на неразтворимия CaSO4. Водният разтвор на хипофосфорната киселина се концентрира при понижено налягане. Вместо калциев хидроксид може да се използва концентрирана барита вода. Чрез третиране на натриев хипофосфит, NaH2PO2 с йонообменна смола. Натриевата сол може да се получи чрез кипене на бял фосфор с разтвор на натриев хидроксид, реакция, подобна на (1) по-горе. PH3 + 2I2 + 2H2O → H3PO2+ 4Здравей Горният метод може да се счита за по-безопасен от този, включващ нагряване на бял фосфор с алкали. Хипофосфорната киселина трябва да се съхранява под 50 градуса. Продава се в търговската мрежа като воден разтвор в различни концентрации. |
| Производствени методи | Хипофосфорната киселина се образува чрез реакция на бариев хипофосфит и сярна киселина и филтриране на бариев сулфат. Чрез изпаряване на разтвора във вакуум при 80 градуса и след това охлаждане до 0 градуса, хипофосфористата киселина кристализира. |
| Определение | ChEBI: Фосфорна оксокиселина, която се състои от един петвалентен фосфор, ковалентно свързан чрез единични връзки с два водорода и хидрокси група и чрез двойна връзка с кислород. Родител на класа фосфинови киселини. |
| Определение | Бяло кристално твърдо вещество. Това е едноосновна киселина, образуваща анион Н2PO2– във вода. Натриевата сол, а оттам и киселината, могат да бъдат получени чрез нагряване на жълт фосфор с разтвор на натриев хидроксид. Свободната киселина и нейните соли са мощни редуциращи агенти. |
| Реакции | Хипофосфорната киселина се смесва с вода във всички пропорции и търговската сила е 30% H3PO2. Хипофосфитите се използват в медицината. Хипофосфористата киселина е мощен редуциращ агент, например с меден сулфат образува меден хидрид Cu2H2, кафява утайка, която отделя водороден газ и оставя мед при затопляне; със сребърен нитрат се получава фино раздробено сребро; със сярна киселина дава сяра и малко сероводород; със сярна киселина се получава сярна киселина, която реагира както по-горе; образува манган незабавно с перманганат. |
| Общо описание | Хипофосфорната киселина изглежда като безцветна маслена течност или разхлабващи се кристали с кисела миризма. Плътност 1,439 g / cm3. Точка на топене 26,5 градуса. Вдишването на изпарения дразни или изгаря дихателните пътища. Течността и изпаренията могат да раздразнят или изгорят очите и кожата. |
| Въздушни и водни реакции | Разхлабващ се. Водоразтворим. |
| Профил на реактивност | ХИПОФОСФОРНАТА КИСЕЛИНА се разлага при нагряване до фосфорна киселина и спонтанно запалим фосфин. Окислява се от сярна киселина с отделяне на серен диоксид и сяра. Реагира експлозивно с живачен(II) оксид [Mellor, 1940, Vol. 4, 778]. Реагира бурно с живачен (II) нитрат [Mellor, 1940, Vol. 4, 993]. Неутрализира основите при екзотермични реакции. |
| Опасност | Риск от пожар и експлозия при контакт с окислители. |
| Опасност за здравето | ТОКСИЧЕН; вдишване, поглъщане или контакт с кожата на материала може да причини тежко нараняване или смърт. Контактът с разтопено вещество може да причини сериозни изгаряния на кожата и очите. Избягвайте всякакъв контакт с кожата. Ефектите от контакт или вдишване могат да бъдат забавени. Пожарът може да произведе дразнещи, корозивни и/или токсични газове. Изтичането от вода за контрол на пожара или разреждане може да бъде корозивно и/или токсично и да причини замърсяване. |
| Опасност от пожар | Негоримо вещество само по себе си не гори, но може да се разложи при нагряване, за да произведе корозивни и/или токсични изпарения. Някои са окислители и могат да възпламенят горими вещества (дърво, хартия, масло, дрехи и др.). При контакт с метали може да се отдели запалим водороден газ. Контейнерите могат да експлодират при нагряване. |
| Методи за пречистване | Фосфорната киселина е често срещан замърсител на търговската 50% хипофосфорна киселина. Дженкинс и Джоунс [J Am Chem Soc 74 1353 1952] пречистват този материал чрез изпаряване на около 600 mL в 1L колба при 40o, при понижено налягане (в N2), до обем от около 300 mL. След като разтворът беше охладен, той беше прехвърлен в Ерленмайерова колба с широко гърло, която беше запушена и оставена в баня със сух лед/ацетон за няколко часа, за да замръзне (ако е необходимо, с надраскване на стената). Когато след това колбата беше оставена при около 5o за 12 часа, около 30-40% от нея се втечни и отново беше филтрирана. Този процес се повтаря, след което твърдото вещество се съхранява върху Mg(ClO4)2 във вакуумен ексикатор на студено. Последващите кристализации от n-бутанол чрез разтварянето му при стайна температура и след това охлаждане в ледено-солна баня при -20o изглежда не го пречистват допълнително. Свободната киселина образува разхлабващи се кристали m 26.5o и е разтворима в H2O и EtOH. Солта NaH2PO2 може да бъде пречистена чрез анионобменна смола [Klement Z Anorg Allgem Chem 260 267 1949.] |
| Продукти и суровини за получаване на хипофосфорна киселина |
| Суровини | AMBERLITE(R) IRC-50 |
| Продукти за приготвяне | XANTHURENIC ACID-->3,5-diisopropylphenol-->cmtirust agent T-708-->Sodium hypophosphite-->TRIS(2,2'-BIPYRIDYL)RUTHENIUM(II) CHLORIDE HEXAHYDRATE-->4-IODOPYRIDINE-2-CARBOXYLIC ACID-->2,3,5,6-Tetrafluorophenol-->Benzothiazole, 4-methyl- (7CI,8CI,9CI)-->BEHENIC ACID METHYL ESTER-->Фосфорна киселина |
Популярни тагове: хипофосфорна киселина, Китай хипофосфорна киселина производители, доставчици, фабрика
Един чифт: Калиев бромат
Следваща: Флуороборна киселина
Може да харесаш също
Изпрати запитване



